
 Portada
España
Investigación
Opinión
Medios
Chismógrafo
Andalucía
Castilla y León
Castilla-La Mancha
C. Valenciana
Economía
Deportes
Motor
Sostenibilidad
Estilo
esTendencia
Salud
ESdiario TV
Viajar
Mundo
Suscribirse
Portada
España
Investigación
Opinión
Medios
Chismógrafo
Andalucía
Castilla y León
Castilla-La Mancha
C. Valenciana
Economía
Deportes
Motor
Sostenibilidad
Estilo
esTendencia
Salud
ESdiario TV
Viajar
Mundo
Suscribirse
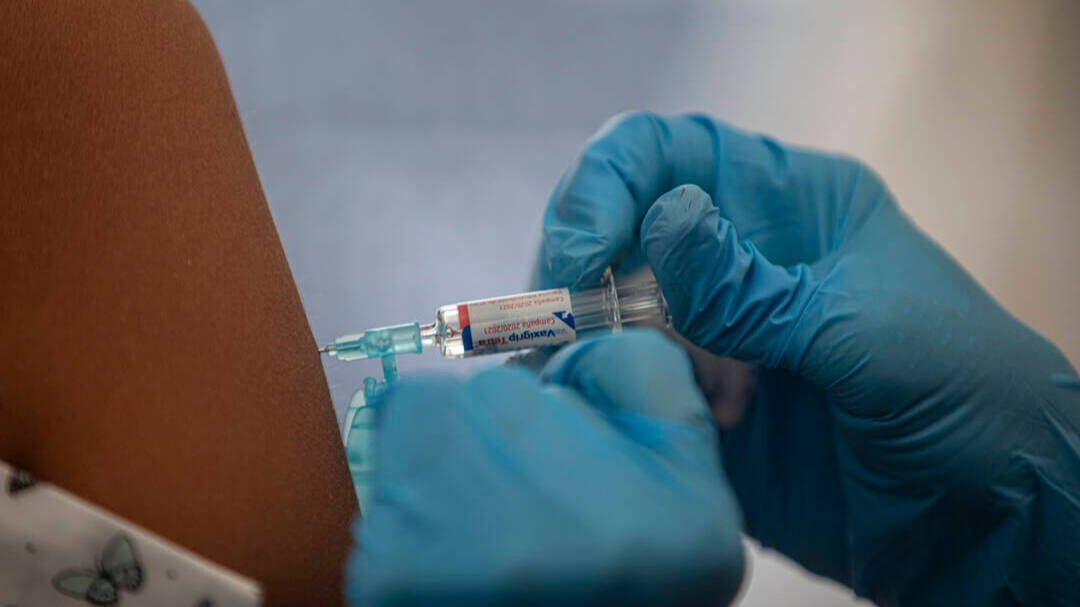
Llega otra esperanza contra el COVID, la vacuna de Moderna es eficaz al 94%
Tras el anuncio de la farmaceútica Pfizer, ahora es la firma biotecnológica estadounidense la que ha anunciado un remedio para inmunizar a la población.
La carrera por tener una vacuna eficaz para acabar con la pandemia de coronavirus sigue adelante. Si hace tan solo una semana era la farmacéutica Pfizer la que anunciaba que su remedio estaba dando resultados prometedores, ahora ha sido el gigante biotecnológico Moderna el que ha conseguido que su efectividad sea del 94,5%.
Así, una nueva esperanza se suma a la anunciada la semana pasada, después de que Moderna haya avanzado estos datos tras un análisis interno de las pruebas en su fase III, correspondientes a 95 personas con casos confirmados de Covid-19. Según han detallado, este caso, 90 participantes en el grupo de placebo contrajeron el la enfermedad, frente a los 5 en el grupo vacunado.

Según las previsiones de la compañía, su intención es producir 20 millones de dosis de su vacuna experimental para finales de año, y tendrá un precio de 25 dólares en Estados Unidos, donde solicitarán una autorización de uso de emergencia en "las próximas semanas".
Sin embargo, su apuesta es mucho más ambiciosa ya que espera tener entre 500 millones y mil millones de dosis en 2021, divididas entre sus sitios de fabricación estadounidenses e internacionales y dependiendo en parte de la demanda, por lo que podría paliar gran parte de la pandemia.
Su administración consistirá en dos inyectables con 28 días de diferencia y su principal ventaja respecto a la de Pfizer es la conservación, (de 2 a 8 grados la de Moderna, frente a los -20 de la de Pfizer), lo que facilitará su distribución.
Además, la Agencia Europea de Medicamentos también ha comenzado su propia revisión de la vacuna, con la intención de que una vez se hayan evaluado todos los datos de los ensayos clínicos que ha ido remitiendo la empresa y de las conclusiones posteriores, se pueda comercializar cuanto antes.
Así, el órgano europeo ha decidido iniciar este proceso basándose "en resultados preliminares de estudios no clínicos y estudios clínicos iniciales en adultos que sugieren que la vacuna desencadena la producción de anticuerpos y células T (células del sistema inmunológico, defensas naturales) que se dirigen al virus", indica la Agencia en un comunicado.